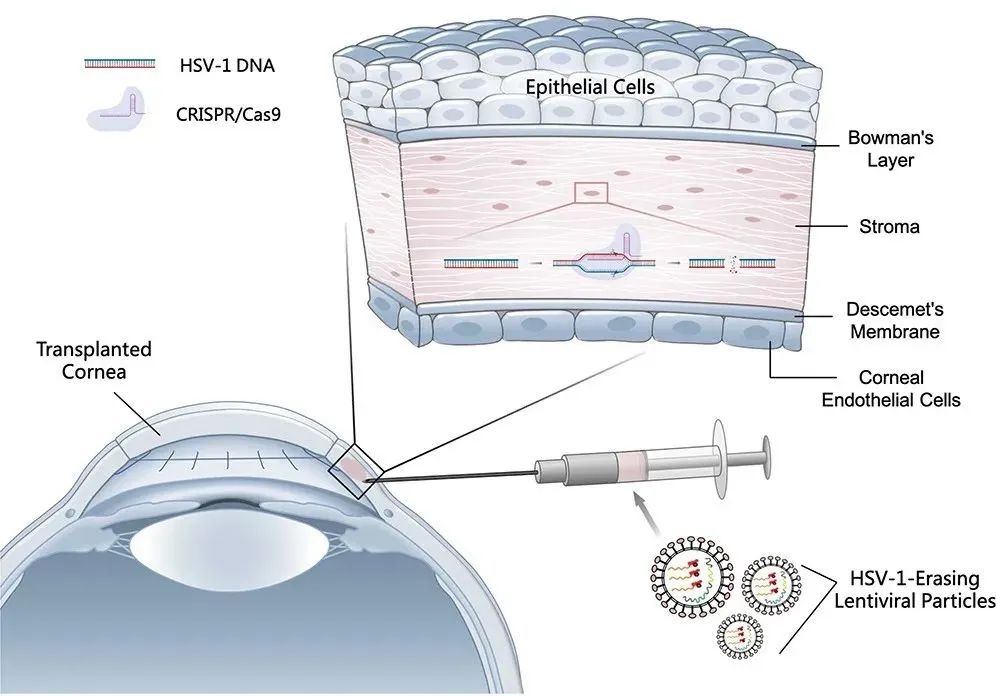
图/对单纯疱疹病毒性角膜炎(HSK)患者进行HELP基因编辑治疗联合角膜移植 来源/MolecularTherapy
2023年8月29日,国务院印发的《河套深港科技创新合作区深圳园区发展规划》正式对外发布之后,深港协同创新进一步加速联通。9月7日,香港科学园深圳分园正式开园,香港应用科技研究院、大湾区创飞学院、大湾区创科快线等首批16家香港科创机构、企业入驻。河套合作区科创项目批量签约入驻。
参考信息>>https://www.gov.cn/zhengce/content/202308/content_6900742.htm
❖ 财政部、商务部、税务总局发布《关于研发机构采购设备增值税政策的公告》
2023年8月28日,财政部、商务部、税务总局联合发布《关于研发机构采购设备增值税政策的公告》,为鼓励科学研究和技术开发,促进科技进步,继续对内资研发机构和外资研发中心采购国产设备全额退还增值税。
❖ 国家卫生健康委发布《出生缺陷防治能力提升计划(2023-2027年)》
2023年8月24日, 国家卫生健康委官网发布《出生缺陷防治能力提升计划(2023-2027年)》,计划到2027年,建立覆盖城乡居民,涵盖婚前、孕前、孕期、新生儿和儿童各阶段,更加完善的出生缺陷防治网络,显著提升出生缺陷综合防治能力。
❖ 北京市人民政府办公厅发布《北京市促进未来产业创新发展实施方案》
2023年9月5日,北京市人民政府办公厅发布《北京市促进未来产业创新发展实施方案》,该方案提出面向未来信息、未来健康、未来制造等六大领域,打造未来产业策源高地。其中,面向未来生命健康和医疗需求,在海淀、石景山、通州、昌平、大兴、平谷、密云、经开区等区域,重点发展基因技术、细胞治疗与再生医学、脑科学与脑机接口、合成生物等细分产业。
❖ 黑石(上海)完成中国证券投资基金业协会登记
2023年8月21日,黑石集团(香港)有限公司旗下全资子公司黑石(上海)私募基金管理有限公司(简称:黑石(上海))在中国证券投资基金业协会完成登记,业务类型为“QDLP等试点机构”。QDLP即合格境内有限合伙人,指获得QDLP试点资格并获批外汇额度的基金管理企业,在中国境内设立QDLP基金并面向中国境内的合格投资者募集人民币,将募集资金换汇后对境外标的进行投资的制度。黑石(上海)注册地址在上海市静安区,注册资本200万美元。
❖ Illumina董事会任命Jacob Thaysen博士为新任CEO
2023年9月5日,DNA测序提供商Illumina宣布其董事会已任命Jacob Thaysen博士,原安捷伦科技高级副总裁、生命科学与应用市场集团总裁,为公司首席执行官,该任命将于2023年9月25日生效。
❖ 基因编辑公司舒桐医疗完成A轮融资
2023年9月5日,珠海舒桐医疗科技有限公司(舒桐医疗)宣布完成A轮融资。本轮融资由陕投成长领投,粤科集团、凯得基金、华诺医疗基金共同参与投资。本轮融资资金将助力舒桐医疗快速推进基因编辑诊断产品商业化和创新药物IND中美申报,不断提升公司技术创新能力。
❖ 合成生物学公司柯泰亚生物完成2.5亿元人民币B轮融资
近日,合成生物学公司上海柯泰亚生物科技有限公司(柯泰亚生物)完成2.5亿元人民币B轮融资,由恒旭资本和斯道资本联合领投,河南汇融、食芯资本跟投,元启资本担任独家财务顾问。柯泰亚生物成立于2021年9月,近2年时间内完成四轮融资,累计融资规模近5亿元人民币。
连续六年发布基因行业蓝皮书后
基因慧启动《细胞和基因治疗蓝皮书》
欢迎学会、园区及企业合作联合发布
邮箱:info@genonet.cn
电话:400-088-0992

2023年9月7日,复旦大学/上海国际人类表型组研究院联合中国计量科学研究院,国家卫健委临床检验中心共同研发的全球首套多组学标准物质“中华家系1号”的最新研究成果在Nature Biotechnology期刊发布。同期2篇论文分别聚焦:“使用基于中华家系1号标准物质的相对定量进行多组学数据整合”和“中华家系1号 RNA标准物质与基于比值的分析方法提高了转录组数据的质量”。这标志着中国科学界自主研制、获批为“国家一级标准物质”的“中华家系1号(Quartet)”多组学标准物质的研发和效用得到了国际同行的认可,开创了生物医学“度量衡”新体系。
❖ 国内首个基因编辑治疗病毒性角膜炎临床结果公布
2023年8月31日,复旦大学附属眼耳鼻喉科医院洪佳旭主任医师与上海交通大学系统生物医学研究院蔡宇伽研究员在MolecularTherapy期刊发表研究论文。该研究对3名伴有急性角膜穿孔的单纯疱疹病毒性角膜炎(HSK)患者进行了HELP治疗联合角膜移植,通过18个月的随访,3名患者均未发生单纯疱疹病毒1型(HSV-1)复发,且没有检测到CRISPR诱导的脱靶效应。HELP瞬时靶向基因编辑技术使用类病毒载体(VLP),以mRNA形式递送CRISPR-Cas9基因编辑工具,Cas9酶在体内停留时间短,可降低脱靶风险、减少免疫反应。
2023年9月8日,默沙东宣布其PD-1抑制剂帕博利珠单抗(商品名:可瑞达®)已获得NMPA批准用于不可切除或转移性微卫星高度不稳定型(MSI-H)或错配修复基因缺陷型(dMMR)成人晚期实体瘤患者,其中包括既往接受过氟尿嘧啶类、奥沙利铂和伊立替康治疗后疾病进展的结直肠癌患者,及既往治疗后疾病进展且无满意替代治疗方案的其他实体瘤。此次新适应证的获批是基于全球II期临床试验KEYNOTE-158和KEYNOTE-164的数据。
❖ 华大智造DNBSEQ-G99基因测序仪获批NMPA医疗器械注册证
2023年9月6日,华大智造基因测序仪DNBSEQ-G99获批国家药品监督管理局(NMPA)医疗器械注册证(国械注准20233221289)。基于DNBSEQ核心技术,G99在测序载片上采用了三角形矩阵式信号位点,在更小面积的载片上实现更高密度的数据产出,整机通量8-48Gb。12小时可完成PE150测序,做到快速、简单、灵活,支持临床方向多种DNA和RNA基因检测应用需求。
❖ FDA批准23andMe的BRCA1/2检测试剂盒升级版,新增41种变异
2023年8月31日,基因检测公司23andMe宣布其获得FDA 510(k) 批准,以扩展其现有的 BRCA1/BRCA2(选定变体)遗传健康风险报告。此次许可使在报告中表达出BRCA1和BRCA2基因中的另外41个变异,这些变异已知与乳腺癌、卵巢癌、前列腺癌和胰腺癌的较高风险相关。此试剂盒初始版本于2018年首次获得FDA授权,进行直接面向消费者的癌症风险基因测试,报告BRCA1和BRCA2基因的3种变异。
❖ 诺华BRAF/MEK组合获FDA批准新适应症
近日,美国FDA官网显示,诺华的Tafinlar(dabrafenib,达拉非尼)+ Mekinist(trametinib,曲美替尼)组合已获批准扩大适应症,适用人群扩大至1岁及以上(原先为6岁及以上)伴有BRAF V600E突变的不可切除或转移性实体瘤人群,这些患者既往接受治疗后疾病发生进展,且没有令人满意的替代治疗方案。
参考信息>>
https://mp.weixin.qq.com/s/m23IxaDaQw0R-cH1tyqT8A
❖ 第十届全国功能基因组学高峰论坛(FGC-10),山东青岛,2023年10月23-27日
参考信息>>
https://mp.weixin.qq.com/s/NhgSj0-dtpRUB0-nq95feQ
❖ 第三届中国生物物理学会代谢组学分会年会暨2023年代谢组学国际研讨会,福建厦门,2023年10月27—29日
参考信息>>
https://meeting.bsc.org.cn/CSM2023
❖ 第十二届全国生物信息学与系统生物学学术大会,山东青岛,2023年10月27-30日
参考信息>>
f550adb41f75e9ebac578ccd19f5dedd_391df430f174284f7b41449ac2c1bff9_8.pdf
【声明】为了推动基因及数字生命健康科技推广、产业发展及政产学研用连接,基因慧秉持专业、赋能、中立的立场收集、分析及发布相关信息。但由于时效性及行业特殊性,所刊登内容仅供研究参考,未经说明不作为决策依据;本文相关信息不代表基因慧的观点;基因慧平台刊登的原创内容的知识产权为“基因慧”商标拥有者及相关权利人所有;欢迎转载,转载请申请并注明来源。欢迎个人及机构投稿及合作。
更多阅读>>
