前列腺癌精准医疗开启,PARP抑制剂的伴随诊断标准化是前提
【导语】2020年,FDA连续批准多款PARP抑制剂,开启了前列腺癌的精准治疗时代,精准治疗的前提是精准检测。目前,PARP抑制剂的常见分子生物标志物已经从 BRCA1/2 发展到 HRR/HRD,国内相关检测刚起步,标准化建设是一件迫在眉睫的工作。
文章 | 菁良基因编辑 | 罗湘
关键词 | 基因检测 标准品
HRR/HRD检测可扩展PARP抑制剂获益人群
上皮性卵巢癌中,17%的患者可检出胚系BRCA1/2突变,体细胞BRCA1/2检测可比胚系BRCA1/2检测增加约7%的检出率,这些患者都是PARP抑制剂治疗的优势人群。
最近,大多数与PARP抑制剂应用相关的主要临床试验均纳入了HRD检测项目并作为分层分析的指标,并发现HRD阳性患者也能获益于PARP抑制剂治疗。
2020年5月11日,FDA批准了奥拉帕利联合贝伐珠单抗用于HRD阳性人群一线维持治疗的适应症。HRD阳性患者占卵巢癌总人群的大约50%,因此HRD检测大大扩展了PARP抑制剂的受益人群。
从2020年5月开始,FDA先后批准了以下2款PARP抑制剂:
卢卡帕利(Rucaparib)用于治疗携带有害BRCA基因突变(胚系和/或体系)的转移性去势抵抗性前列腺癌(mCRPC)成人患者,这也是前列腺癌领域获批的第一款PARP抑制剂。
奥拉帕利(Olaparib)用于治疗携带有害或可能有害的HRR基因突变(胚系或体系)的mCRPC成人患者。
PARP抑制剂在mCRPC患者中的生物标志物便从BRCA1/2两个基因拓宽到了HRR一系列基因(包括BRCA1/2),即从12%的mCRPC人群扩展到25%的mCRPC人群,PARP抑制剂的获益人群也近乎增加了一倍。
FDA批准的HRR/HRD检测
FDA在批准奥拉帕利的同时分别批准了FMI(Foundation Medicine, Inc.)的 FoundationOne CDx(F1CDx)及 Myriad 的 BRACAnalysis CDx 作为其伴随诊断产品,分别检测组织HRR基因突变及血液gBRCA1/2基因突变。
目前,在HRD检测上经过临床验证且获FDA批准的只有两个产品,Myriad Genetics myChoice Test和FoundationOne CDx(FDA批准用于检测gLOH)。2020年4月22日,FoundationOne®CDx(F1CDx)卵巢癌报告中增加基因组杂合性缺失(gLOH)检测功能,成为国内首个可以判断同源重组修复缺陷(HRD)的商用NGS产品,然而Myriad Genetics myChoice Test在国内尚不可及。
国内HRD检测产品则刚刚起步,尚没有NMPA批准的产品,不过各大肿瘤基因检测公司也在积极布局HRD产品的开发与申报。
HRR/HRD检测最新相关指南和共识
1. 在2020前列腺癌NCCN指南Principles of Genetics部分,明确推荐转移性前列腺癌患者进行体细胞变异的检测,包含的HRR基因有BRCA1、BRCA2、ATM、PALB2、FANCA、RAD51D、CHEK2和CDK12。对于局部晚期的患者也可以考虑进行HRR基因检测。
2. 《中国前列腺癌患者基因检测专家共识(2020年版)》指出对于所有mCRPC患者,推荐进行至少包含HRR基因胚系及体系变异的检测,并可以考虑行微卫星不稳定性(microsatellite instability,MSI)和DNA错配修复缺陷(DNA mismatch repair deficiency,dMMR)检测。
3. 在2020年最新版NCCN卵巢癌指南中提到,对复发卵巢癌患者除进行BRCA1/2突变和微卫星不稳定或DNA错配修复(若既往未行检测)外,还可评估HRD状态。若无BRCA1/2突变,HRD检测可以提供信息帮助判断患者从PARP抑制剂治疗获益的程度。
4. 《2020版卵巢上皮性癌维持治疗中国专家共识》也推荐,初治卵巢癌患者在获得病理确诊后,在条件允许情况下评估HRD状态。这无疑对临床检测提出了新的要求,需要具有临床指导意义的HRD检测方法,帮助临床医生为患者制定个体化的治疗方案。
5. 2020月11月13日发布的《上皮性卵巢癌PARP抑制剂相关生物标志物检测的中国专家共识》中也表示:HRD作为卵巢癌治疗相关的重要生物标志物,对含铂化疗和PARP抑制剂反应高度敏感,新诊断的卵巢癌患者,应积极进行HRD等相关生物标志物的检测。
推动国内HRR/HRD检测标准化建设迫在眉睫
PARP抑制剂开启了前列腺癌的精准治疗时代,而HRR的准确检测是保证精准用药的前提。统计数据显示我国前列腺癌患者5年生存率仅为69.2%,而美国前列腺癌患者的5年生存率达到了99%,我国的前列腺癌精准治疗仍然是任重而道远。
今年由中国健康促进与教育协会发起的“精泌前行暨HRR检测校准项目”也旨在希望通过HRR检测校准项目推动相关基因检测技术的完善、检测标准的建立,同时呼吁临床、病理、检验专家共同协作,助力前列腺癌精准诊疗。
HRD检测对于指导卵巢癌的治疗十分重要,临床对HRD检测的需求将会越来越大,HRD检测目前不论在国内外均无统一标准,可以开展检测的实验室也屈指可数。虽然目前国内有很多医院和第三方可以提供BRAC基因检测服务,但每个实验室检测质量不一致,都会影响到最终结果的准确性,为临床诊疗活动带来极大困扰。HRD的检测及标准化建设是一件迫在眉睫的工作。
菁良解决方案>>HRR标准品<<
菁良基因HRR标准品包含与HRR通路相关的基因突变,可定制gDNA,ctDNA 或者 FFPE等产品形式,是HRR检测试剂盒注册报证及HRR检测日常质控理想的参考品。
产品特点
细胞系来源:更接近临床样本
覆盖HRR通路大部分基因:>24 个HRR相关基因,>170 个突变位点
可定制Pathogenic,likely Pathogenic, VUS, likely benign, benign多种临床意义的突变位点
灵活的定制方案:可混合特定的突变位点,及选择对应突变频率至一个产品
突变频率可定制范围广:0%-100%
多种产品形式可选:gDNA、ctDNA、FFPE
位点经ddPCR验证:绝对定量AF
>>HRD标准品<<
如果CDx Panel中HRD状态是通过检测基因组瘢痕,也可选择菁良提供的通过HRD 基因组瘢痕的检测方法来评估HRD状态的标准品。例如通过LOH,LST,TAI的综合评分,来计算HRD 分值。同时,菁良基因也可提供HRD panel性能验证的各种参考品,例如特异性,灵敏性,精密度,抗干扰能力验证参考品。
产品特点
通过开源的生信流程对LOH,LST,TAI的综合评分
HRD score 分布广
可提供配对的HRD标准品,可更好计算HRD score
细胞系来源,最大限度模拟临床样本
多种产品形式可选:gDNA、ctDNA、FFPE
质量认证:ISO9001
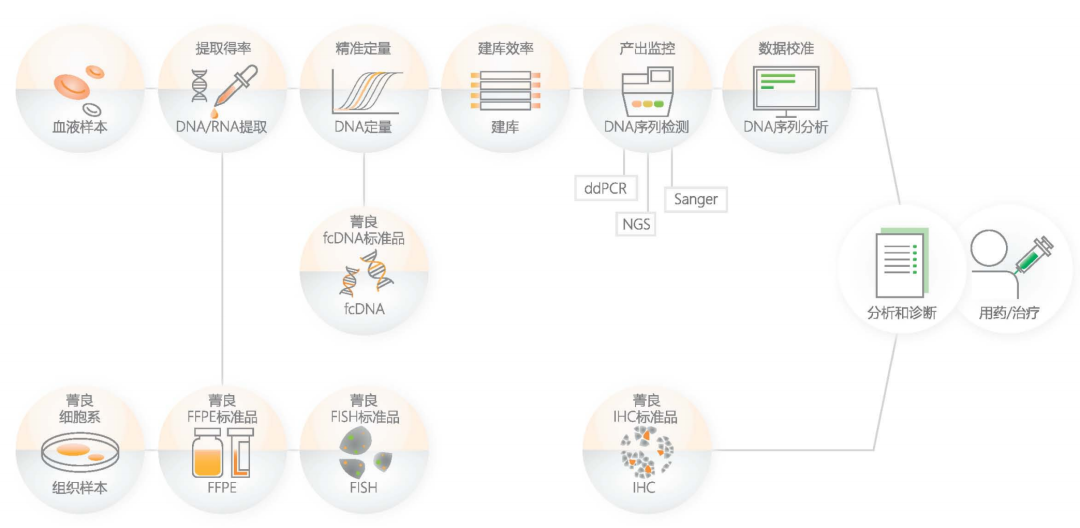
图:分子诊断标准品全流程监控(来源/菁良基因)
附:关于HRR/HRD检测
什么是同源重组修复通路基因(HRR)?
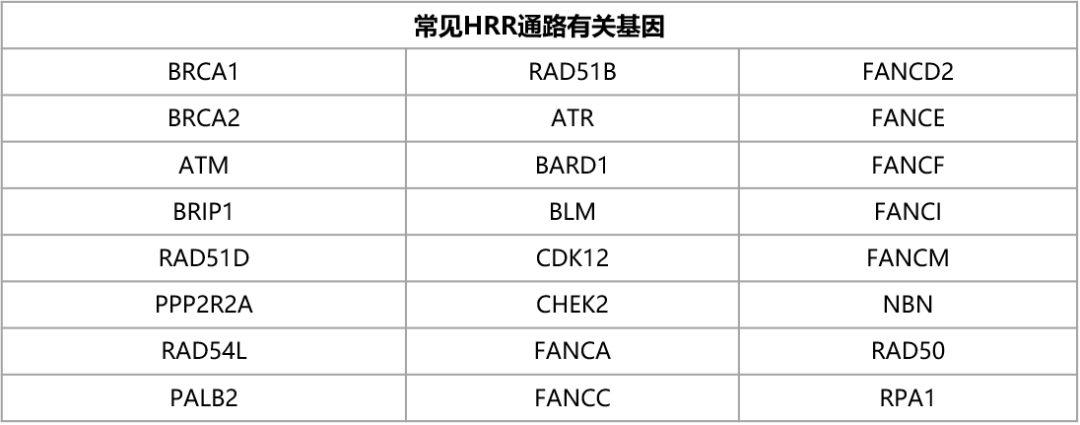
除了最著名的BRCA1/2,同源重组修复通路还包括上下游调控的众多基因,它们同样也在DNA双链断裂的修复中起到重要作用。目前比较公认的有华盛顿大学16个基因的HR panel(基因列表:ATM, ATR, BARD1, BLM, BRCA1, BRCA2, BRIP1, CHEK2, MRE11A, NBN, PALB2, RAD51C, RAD51D, RBBP8, SLX4, XRCC2)。
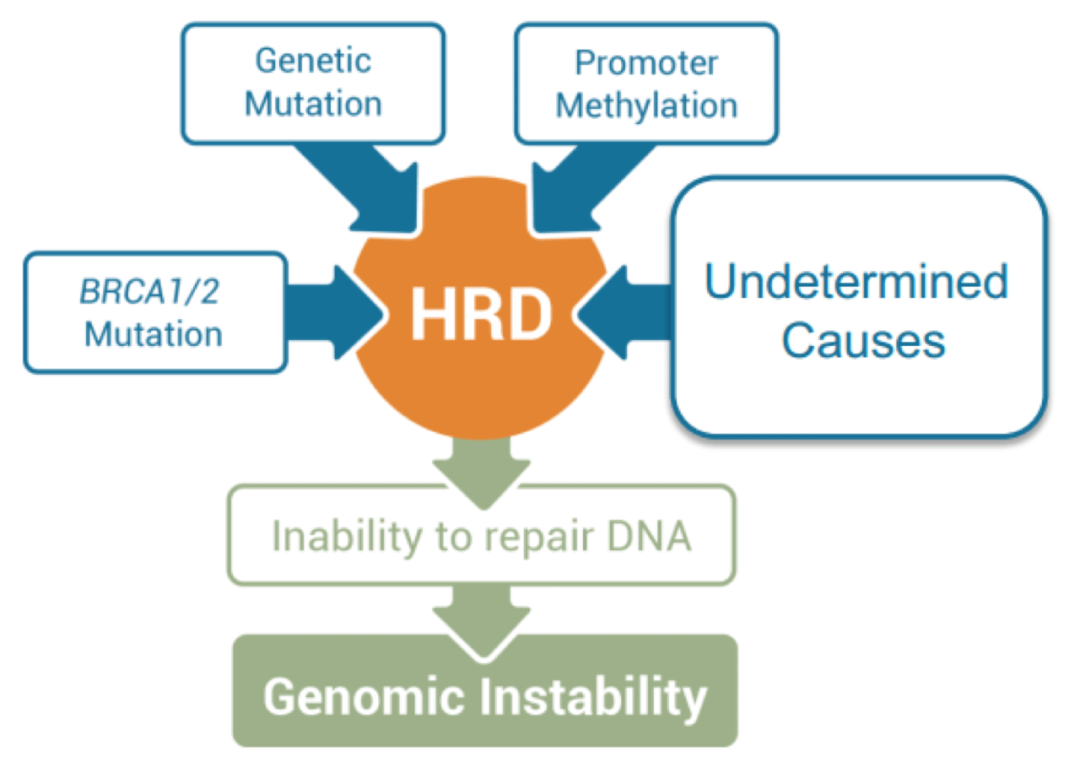
图:HRD发生原因(来源/Google)
什么是同源重组修复缺陷(HRD)?
HRD指的就是当DNA出现双链断裂时,细胞失去了通过同源重组的方式对断裂进行修复的能力。导致HRD的原因是多方面的,目前已知的原因除了BRCA1/2基因发生突变外,BRCA1启动子甲基化、HRR其他基因突变以及外界因素导致的BRCA基因表达下调都会导致HRD。
当前组织检测仍是HRR检测的金标准,FDA已经批准组织检测作为前列腺癌HRR基因突变的伴随诊断。在组织检测失败或不可及的情况下,可以考虑使用血浆ctDNA的检测方式。国外相关研究显示,在满足一定的ctDNA丰度和检测深度的情况下,血浆ctDNA与组织检测的一致性能够达到80-90%,两者间的一致性有待更进一步的探索和确诊。
HRD检测尚无统一标准,主要有两种途径:
HRR Gene Panel:通过检测关键HRR基因突变来评估产生HRD的原因
HRD Genomic Scar:通过检测基因组损伤的模式来鉴定HRD的结果
目前报道的卵巢癌PARPi相关研究主要选择使用HRD Genomic Scar法鉴定HRD,即:HRD将以一种特定且可识别的方式标记(或损伤)基因组疤痕。HRD Genomic Scar不仅可以检测BRCA状态,还可以分析基因不稳定状态类型。基因不稳定状态类型分为三种类型:基因组杂合性丢失(LOH, Loss of heterozygosity)、端粒等位基因失平衡(TAI, Telomeric allelic imbalance)和大片段迁移(LST,Large-scale state transitions) 。
参考资料:
[1] Li X, Heyer WD. Homologous recombination in DNA repair and DNA damage tolerance. Cell Res. 2008;18:99-113.
[2] Lord CJ, Ashworth A. BRCAness revisited. Nat Rev Cancer. 2016;16:110-120. [3] Watkins JA, Irshad S, Grigoriadis A, Tutt AN. Genomic scars as biomarkers of homologous recombination deficiency and drug response in breast and ovarian cancers. Breast Cancer Res. 2014;16:211
[4]NCCN Guideline Ovarian Cancer (2020.V1).
[5]中国抗癌协会妇科肿瘤专业委员会.中国卵巢上皮性癌维持治疗专家共识(2020). 中国实用妇科与产科杂志.2020;36(3):234-238.
[6]中国抗癌协会妇科肿瘤专业委员会.中华医学会病理学分会.上皮性卵巢癌PARP抑制剂相关生物标志物检测的中国专家共识. 《中国癌症杂志》.2020.30(10):841-848.
[7]NCCN Guidelines Version 1.2020 Prostate Cancer
[8]中国抗癌协会泌尿男生殖系肿瘤专业委员会,中国临床肿瘤学会前列腺癌专家委员会. 中国前列腺癌患者基因检测专家共识(2020年版)[J]. 中国癌症杂志, 2020, 30(7): 551-560.
推荐阅读
月
【声明】为传播科学信息,推动基因及数字生命健康产学研连接,我们秉持中立、专业、赋能的理念收集、分析或发布信息。但由于时效性及行业特殊性,所刊登内容仅供研究参考,不作为决策依据;本文相关信息不代表基因慧机构的观点;“基因慧”刊登的原创内容的知识产权为“基因慧”商标拥有者及相关权利人所有;欢迎转载,转载请申请并注明来源。欢迎个人及机构投稿及合作。
关于基因慧
基因慧是数字生命健康领域创新服务平台。团队深耕行业十余年,从行研咨询、媒体资讯、产业平台等角度提供优质内容。作为国发改产业研究合作单位,基因慧联合多家头部机构连续四年发布公开的行研报告,为产业园、投资机构、头部企业及政府提供咨询规划服务,参与组织发布行业共识和标准,致力于建设数字生命健康产业数字化平台,服务生命科技创新创业。
☆ 中国遗传学会生物产业促进委员会委员
☆ 受邀为
华西、
Illumina、
华大、
上海交大等报告
☆ 广东省精准医学应用学会政策研究应用分会常务委员